Cili prodhim bazohet në reagimin e pasqyrës së argjendit. Eksperiment kimik: marrja e një pasqyre argjendi
Përfundimi i punës:
Në një epruvetë u hodh 1 ml formalinë dhe u shtua pak tretësirë amoniaku e oksidit të argjendit. Provëza u ngroh. Vëzhgojmë depozitimin e argjendit në muret dhe në fund të epruvetës. Sipërfaqja e xhamit bëhet reflektuese, sepse ky është parimi i bërjes së pasqyrave.
Eksperimenti 2. Oksidimi i benzaldehidit me oksigjenin atmosferik
Përfundimi i punës:
Një pikë benzaldehidi u vendos në një rrëshqitës xhami dhe u la në ajër për 30 minuta. Ne vëzhgojmë formimin e kristaleve të bardha përgjatë skajeve të rënies. Ndodhi një reaksion oksidimi dhe u formua acidi benzoik.

Eksperimenti 3. Përgatitja e acetonit nga acetati i natriumit
Pak pluhur natriumi acetat u vendos në epruvetë dhe u mbyll me një tapë me një tub për daljen e gazit. Provëza u montua në një stendë. Fundi i tubit të daljes së gazit u ul në një provëz me ujë. Një epruvetë që përmbante acetat natriumi u ngroh. Vëzhgojmë lëshimin e flluskave të gazit në një epruvetë me ujë dhe ndihet era specifike e acetonit. Pasi reaksioni të ndalet, shtoni një pikë acid klorhidrik të koncentruar në epruvetën e parë. Ne vëzhgojmë lëshimin e flluskave të dioksidit të karbonit.
Eksperimenti me efektin e bukur të formimit të një shtrese pasqyre në xhami është shumë vizual. Ky reagim kërkon përvojë dhe durim. Në këtë artikull do të mësoni për përgatitjen e nevojshme dhe specifike të pajisjeve, dhe gjithashtu do të shihni se cilat ekuacione reagimi ndodh ky proces.
Thelbi i reaksionit të pasqyrës së argjendit është formimi i argjendit metalik si rezultat i një reaksioni redoks gjatë bashkëveprimit të një solucioni amoniaku të oksidit të argjendit në prani të aldehideve.
"Pasqyra e argjendtë" (epruvetë në të majtë)Për të krijuar një shtresë argjendi të qëndrueshme do t'ju duhet:
- balonë qelqi me një kapacitet deri në 100 ml;
- zgjidhje amoniaku (2,5-4%);
- nitrat argjendi (2%);
- tretësirë ujore e formaldehidit (40%).
Në vend të kësaj, ju mund të merrni një reagent Tollens të gatshëm - një zgjidhje amoniaku e oksidit të argjendit. Për ta krijuar atë, duhet të shtoni 1 gram nitrat argjendi në 10 pika ujë (nëse lëngu do të ruhet për një kohë të gjatë, duhet ta vendosni në një vend të errët ose në një enë qelqi me mure të errëta). Menjëherë para eksperimentit, tretësira (rreth 3 ml) duhet të përzihet në një raport 1:1 me një tretësirë ujore 10% të hidroksidit të natriumit. Argjendi mund të precipitojë, kështu që hollohet duke shtuar ngadalë një zgjidhje amoniaku. Ne rekomandojmë kryerjen e një eksperimenti tjetër spektakolar me një zgjidhje amoniaku dhe shtypjen e një "fotografie kimike".
Reagimi kryhet në temperaturën e dhomës. Një parakusht për një finale të suksesshme janë muret krejtësisht të pastra dhe të lëmuara të enës së qelqit. Nëse ka grimcat më të vogla të ndotësve në mure, sedimenti i marrë si rezultat i eksperimentit do të bëhet një shtresë e lirshme me ngjyrë të zezë ose gri të errët.
Për pastrimin e balonës duhet të përdorni lloje të ndryshme solucionesh alkali, pra për përpunim mund të merrni një tretësirë, e cila pas pastrimit duhet të lahet me ujë të distiluar. Është e nevojshme të shpëlani balonën e agjentit të pastrimit shumë herë.
Pse është kaq e rëndësishme pastërtia e anijes?
Fakti është se grimcat koloidale të argjendit të formuara në fund të eksperimentit duhet të ngjiten fort në sipërfaqen e xhamit. Në sipërfaqen e tij nuk duhet të ketë grimca yndyrore ose mekanike. uji nuk përmban kripëra dhe është ideal për pastrimin përfundimtar të balonës. Mund të përgatitet në shtëpi, por është më e lehtë të blini lëng të gatshëm.
Ekuacioni i reagimit të pasqyrës së argjendit:
Ag2O + 4 NH3·Н2О ⇄ 2ОН + 3Н2О,
ku OH është hidroksidi i argjendit diamine, i marrë nga tretja e oksidit të metalit në një tretësirë ujore të amoniakut.
 Molekula komplekse e argjendit diaminë
Molekula komplekse e argjendit diaminë
E rëndësishme! Reagimi funksionon në përqendrime të ulëta të amoniakut - vëzhgoni me kujdes përmasat!
Kështu vazhdon faza e fundit e reagimit:
R (çdo aldehid)-CH=O + 2OH → 2Ag (koloid argjendi i precipituar) ↓ + R-COONH4 + 3NH3 + H2O
Është më mirë të kryeni fazën e dytë të reagimit duke ngrohur me kujdes balonën mbi flakën e djegësit - kjo do të rrisë shanset që eksperimenti të jetë i suksesshëm.
Çfarë mund të tregojë reagimi i një pasqyre të argjendtë?
Ky reaksion kimik interesant jo vetëm që demonstron gjendje të caktuara të një substance - ai mund të përdoret për të kryer një përcaktim cilësor të aldehideve. Kjo do të thotë, një reagim i tillë do të zgjidhë pyetjen: nëse ka një grup aldehidi në zgjidhje apo jo.
 Formula e përgjithshme strukturore e aldehideve
Formula e përgjithshme strukturore e aldehideve
Për shembull, në një proces të ngjashëm mund të zbuloni nëse një zgjidhje përmban glukozë ose fruktozë. Glukoza do të japë një rezultat pozitiv - do të merrni një "pasqyrë argjendi", por fruktoza përmban një grup keton dhe është e pamundur të merret një precipitat argjendi. Për të kryer analizën, në vend të një solucioni formaldehidi, është e nevojshme të shtoni një zgjidhje 10% të glukozës. Le të shohim pse dhe si argjendi i tretur shndërrohet në një precipitat të ngurtë:
2OH + 3H2O + C6H12O6 (glukozë) = 2Ag↓+ 4NH3∙H2O + C6H12O7 (formohet acidi glukonik).
Është e nevojshme të kuptohet se cili është reagimi i pasqyrës së argjendit? Reagimi i pasqyrës së argjendit është procesi i reduktimit të argjendit metalik nga një zgjidhje amoniaku e oksidit të argjendit.
Ag2O + 4NH4OH ↔ 2OH + H2O
Oksidi i argjendit në një tretësirë ujore të amoniakut shpërndahet për të formuar një përbërje komplekse argjendi - hidroksid diamine argjendi (I) OH.
Duke shtuar ndonjë aldehid (formaldehid) në një përbërje komplekse argjendi, argjendi metalik formohet si rezultat i një reaksioni oksido-reduktues. Si rezultat i reagimit, një shtresë e bukur pasqyre prej argjendi ose një pasqyre do të formohet në muret e epruvetës së qelqit.
R-CH=O + 2OH → 2Ag ↓ + R-COONH4 + 3NH3 + H2O
Në çdo libër shkollor të kimisë mund të lexoni se reaksioni i pasqyrës së argjendit mund të përdoret për të zbuluar aldehidet. Për shembull, glukoza jep një reagim "pasqyrë argjendi", por fruktoza jo. Megjithatë, ka shumë kimikate që, si aldehidet, mund të reagojnë me pasqyrën e argjendit.
Si mund ta kryeni reagimin e pasqyrës së argjendit në praktikë?
Në pamje të parë, duket se është shumë e lehtë të realizosh reagimin e pasqyrës së argjendtë, por kjo nuk është plotësisht e vërtetë. Gjithçka dukej e thjeshtë, ju mund të merrni një zgjidhje amoniaku me pak aldehid, mund të jetë një zgjidhje formaldehidi ose glukoze dhe të kryeni reagimin e pasqyrës së argjendit. Sidoqoftë, kjo është një qasje e thjeshtë dhe primitive për të kuptuar se çfarë është reagimi i pasqyrës së argjendit? Ky reagim mund të çojë në zhgënjim. Në vend të shtresës së pritshme të pasqyrës në xhami, mund të formohet një pezullim i zi ose kafe i argjendit në tretësirë.Zakonisht reagimi në një mënyrë kaq të thjeshtë përfundon me dështim në shumicën e rasteve. Edhe nëse arrijnë të krijojnë një pasqyrë, ajo do të jetë e cilësisë shumë të ulët. Shtresa e argjendit rezulton të jetë e brishtë dhe e pabarabartë. Pse po ndodh kjo? Ka shumë arsye për një reagim të tillë të pasuksesshëm. Nga këto, mund të dallohen dy arsye kryesore: mospërputhja me kushtet e nevojshme për reagimin ose një sipërfaqe qelqi e përgatitur keq për argjend.
Si rezultat i reaksionit, formohet një jon argjendi i ngarkuar pozitivisht, i cili kombinohet me grupin aldehid për të formuar grimca të vogla ose koloidale argjendi. Grimca të tilla të vogla mund të ngjiten fort në sipërfaqen e xhamit ose të mbeten në tretësirë në formën e një pezullimi argjendi.
Në mënyrë që grimcat e argjendit koloidal të ngjiten në mënyrë të besueshme në xhami dhe të formojnë një shtresë të fortë dhe uniforme argjendi, domethënë një pasqyrë, sipërfaqja e qelqit duhet së pari të pastrohet para argjendit. Sipërfaqja e xhamit duhet të jetë jo vetëm krejtësisht e pastër, por edhe sa më e lëmuar.
Ndotësi kryesor i xhamit është yndyra, e cila duhet të hiqet. Për të hequr yndyrën, përdorni një zgjidhje alkali, një përzierje të nxehtë kromi dhe më pas gota lahet vazhdimisht me ujë të distiluar. Nëse nuk ka alkali, mund të përdorni një detergjent të zakonshëm sintetik për larjen e enëve si mjetin e fundit. Pas heqjes së yndyrës, është e dobishme të shpëlani gotën me një zgjidhje të klorurit të kanozit dhe ujit të distiluar.
Të gjitha tretësirat duhet të bëhen me ujë të distiluar. Nëse uji i distiluar nuk është i disponueshëm, si mjet i fundit, mund të përdorni ujin e shiut. Për të reduktuar argjendin metalik në reaksionin e pasqyrës së argjendit, shpesh përdoren agjentë reduktues: formaldehid ose glukozë. Zgjedhja e këtyre dy substancave varet nga qëllimi për të cilin do të përdoret reaksioni kimik.
Reagimi i pasqyrës së argjendit duke përdorur formaldehid
Për të demonstruar eksperimentin, reagimi i një pasqyre argjendi mund të kryhet me pjesëmarrjen e formaldehidit. Nëse keni nevojë të bëni një pasqyrë me cilësi të lartë me një sipërfaqe të qëndrueshme dhe uniforme, është më mirë të përdorni glukozë.Për xhami argjendi, është më mirë të merret argjendi, i cili përmban kripë argjendi - nitrat argjendi. Nitratit të argjendit i shtohen tretësirat e amoniakut dhe alkalit. Depozitimi i argjendit në xhami duhet të bëhet në një zgjidhje alkaline. Në këtë rast, nuk duhet të ketë shumë zgjidhje alkali, pasi teprica e saj është gjithashtu e padëshirueshme. Në varësi të teknikës, reagimi i pasqyrës së argjendit kryhet në temperaturën e dhomës ose kur nxehet.
Kur një tretësirë merr ngjyrë kafe, kjo do të thotë se grimcat e vogla koloidale të argjendit janë formuar në tretësirë. Më vonë, një shtresë e hollë pasqyre me argjend të reduktuar formohet në sipërfaqen e xhamit. Është shumë e lehtë për të kryer reagimin e një pasqyre argjendi, por mund të jetë shumë e vështirë për të marrë një pasqyrë me cilësi të lartë. Për të marrë një shtresë argjendi me cilësi të lartë - një pasqyrë argjendi, duhet të shpenzoni shumë punë, dhe duhet të jeni të kujdesshëm dhe shumë këmbëngulës.
Për eksperiment, ju mund të bëni thjesht një gotë qelqi argjendi, me qëllim të njohjes paraprake dhe të zbuloni se cili është reagimi i një pasqyre argjendi? Kur demonstrohet ky reagim, rezultati mund të jetë një pasqyrë me cilësi jo shumë të mirë.
Për të kryer reaksionin do të na duhen: një balonë qelqi e pastër me një kapacitet 50 - 100 ml, një zgjidhje amoniaku në një përqendrim prej 2.5 deri në 4 përqind, një zgjidhje 2 përqind e nitratit të argjendit dhe një zgjidhje formaldehidi.
Para argjendimit, ne përgatisim balonën për një reaksion kimik. Le ta pastrojmë balonën nga papastërtitë mekanike duke e fshirë me furçë dhe sapun dhe më pas e shpëlajmë balonën me ujë të distiluar. Më pas e shpëlajmë me masën e kromit dhe më pas e shpëlajmë sërish me ujë të distiluar.
Hidhni një tretësirë 2 për qind në një të katërtën e balonës, më pas shtoni gradualisht tretësirën e amoniakut në këtë tretësirë. Një tretësirë amoniaku përgatitet në shkallën e marrjes së një solucioni 25 për qind të amoniakut dhe hollimit të tij me ujë të distiluar 8 deri në 10 herë. Nitratit të argjendit i shtojmë gradualisht tretësirën e amoniakut derisa precipitati që bie të tretet plotësisht në tepricën e tij. Në tretësirën që është formuar, gradualisht shtoni një zgjidhje të formalinës - 0,5 - 1 ml përgjatë murit. E vendosim balonën e qelqit në një enë me ujë të nxehtë ose edhe më mirë të vluar. Së shpejti do të fillojë të formohet në balonë, e cila formon një pasqyrë të bukur argjendi.
Disavantazhi kryesor i kësaj teknike është se në zgjidhjen e nitratit të argjendit, duhet të shtoni jo vetëm një zgjidhje amoniaku, por edhe një alkali (kjo mund të jetë hidroksid natriumi - NaOH ose hidroksid kaliumi - KOH). Për të marrë një shtresë pasqyre me cilësi të lartë, së pari duhet të shtoni amoniak dhe më pas alkali.
Për të demonstruar thjesht reagimin e një pasqyre argjendi, mund të bëni të kundërtën: së pari shtoni alkali në nitratin e argjendit derisa të ndalojë formimi i një precipitati kafe - (Ag2O), dhe më pas shtoni një zgjidhje amoniaku derisa precipitati të tretet plotësisht:
2Ag+ + 2OH - = Ag2O + H2O
Ag2O + 4NH3 + H2O = 2OH
Gjatë kryerjes së kësaj teknike, mund të formohet një precipitat i bardhë, ka shumë të ngjarë që do të jetë metenaminë (ose heksametilentetraminë):
6CH2O + 4NH3 = (CH2)6N4 + 6H2O
Formimi i një precipitati të bardhë është një shenjë e keqe dhe nuk kontribuon në marrjen e një pasqyre me cilësi të lartë.
Duhet të theksohet veçanërisht se reagimi i një pasqyre argjendi duhet domosdoshmërisht të ndodhë në një mjedis alkalik, dhe jo në një mjedis acid. Në një mjedis acid, reagimi i pasqyrës së argjendit do të bëhet pa formimin e një shtrese argjendi. Ndonjëherë ndodh që gjatë përzierjes së reagentëve, mediumi papritmas bëhet acid. Mjafton të shtohet alkali i tepërt në përzierjen e reaksionit dhe menjëherë në muret e epruvetës së qelqit krijohet një pasqyrë argjendi.
Reagimi i pasqyrës së argjendit duke përdorur glukozë
Reaksioni i pasqyrës së argjendit duke përdorur glukozë mund të kryhet jo vetëm për të demonstruar reaksionin kimik, por edhe për të marrë një pasqyrë argjendi me cilësi të lartë ose sipërfaqe përçuese.Të gjithë e dinë mirë se reaksioni i pasqyrës së argjendit është një proces kimik për reduktimin e argjendit metalik nga një tretësirë amoniaku e oksidit të argjendit (reagent Tollens).
Reaksioni i pasqyrës së argjendit është baza për prodhimin e pasqyrave të argjendta. Për të parandaluar që argjendi metalik (Ag) të oksidohet dhe të formojë ngjyrë të zezë (Ag2S), domethënë, të mos bëhet i shurdhër dhe gërvishtur, ai lyhet me një llak mbrojtës. Për të argjenduar një pasqyrë, duhet të përgatisni dy solucione të sapopërgatitura (A dhe B).
Zgjidhja - A
Në 100 ml ujë të distiluar shpërndahen 6 gram nitrat argjendi - (AgNO3), në këtë tretësirë shtohet tretësira ujore e amoniakut derisa të tretet precipitati i formuar fillimisht. Pastaj shtoni alkali në tretësirën që rezulton - 70 ml tretësirë 3 përqind të hidroksidit të natriumit (NaOH) dhe derdhni përsëri në një tretësirë ujore të amoniakut derisa tretësira të jetë plotësisht e pastër (pa tepricë). Zgjidhja që rezulton hollohet me ujë të distiluar në 500 ml.Zgjidhja - B
Në 25 ml ujë të distiluar shpërndahen 1,3 gram glukozë (tretësit të përftuar i shtohet një pikë acid nitrik i koncentruar - HNO3) dhe tretësirën e përftuar e ziejmë për dy minuta. Më pas ftohni tretësirën dhe holloni me të njëjtin vëllim alkooli.Zgjidhjet: Përzieni A dhe B pak para përdorimit në një raport 10:1. Pas përzierjes së tretësirave, një shtresë e trashë argjendi formohet në gotë brenda 30 minutave.
Para se të argjendoni një pasqyrë, duhet të pastroni mirë xhamin. Ky është një kusht shumë i rëndësishëm dhe i domosdoshëm. Për të marrë një shtresë pasqyre me cilësi të lartë, kjo gjendje nuk mund të neglizhohet. Sipërfaqja e qelqit pastrohet me një përzierje të nxehtë - HNO3 + K2Cr2O7, më pas gota shpëlahet në ujë të distiluar dhe trajtohet me alkool.
Për të përftuar një shtresë më të trashë argjendi, trajtimi sipërfaqësor i xhamit të argjendtë përsëritet përsëri me porcione tretësish të sapopërgatitura, një ose dy herë të tjera. Më pas lahet me ujë dhe alkool, formohet një precipitat argjendi.
Reagimi i pasqyrës së argjendit duke përdorur saharozë
Reagimi i pasqyrës së argjendit mund të kryhet (nëse nuk ka formaldehid ose glukozë) me pjesëmarrjen e saharozës. Para reaksionit, saharoza hidrolizohet duke përdorur acide sulfurik dhe nitrik të holluar në përqendrim 10%. Një tretësirë acidi shtohet në një tretësirë ujore të sheqerit në raport: 10 ml acid për 100 gram sheqer. Ziejeni tretësirën që rezulton për 15-20 minuta. I nënshtruar hidrolizës, saharoza bëhet një përzierje e glukozës dhe fruktozës.Reagimi i pasqyrës së argjendit duke përdorur niseshte
Përdorimi i niseshtës në reaksion në vend të glukozës çon në dështim. Kjo ndodh sepse niseshteja nuk shndërrohet plotësisht në glukozë si rezultat i hidrolizës. Me këtë hidrolizë të pjesshme të niseshtës, formohen dekstrinat - polisaharide, të cilat, si niseshteja, përbëhen nga njësi glukoze që kanë një peshë molekulare më të ulët, ndryshe nga niseshteja. Dekstrinat, në fund të zinxhirëve, kanë grupe aldehide që reduktojnë jonin e argjendit, por kjo prodhon një zgjidhje të zezë koloidale të argjendit, në vend të veshjes së pritshme të pasqyrës. Argjendi metalik nuk vendoset në sipërfaqen e qelqit, me sa duket sepse molekulat e gjata lineare të dekstrineve stabilizojnë tretësirën koloidale të argjendit. Këto molekula, me fjalë të tjera, kryejnë funksionin e një koloidi mbrojtës. Për të parandaluar formimin e një zgjidhjeje të zezë koloidale të argjendit, është e nevojshme hidroliza e plotë e niseshtës.Puna laboratorike nr.5
Vetitëkarbohidratet
Eksperimenti 1. Reagimi i një pasqyre argjendiështë një reagim rikuperimi argjendi nga tretësira e amoniakut oksid argjendi (Reagent Tollens).
Në tretësirë ujore amoniaku oksidi i argjendit shpërndahet për të formuar një përbërje komplekse - hidroksid diamine argjendi (I) OH
kur i shtohet së cilës aldehide ndodh një reaksion redoks për të formuar argjend metalik:
Nëse reaksioni kryhet në një enë me mure të pastra dhe të lëmuara, atëherë argjendi precipiton në formën e një filmi të hollë, duke formuar një sipërfaqe pasqyre.
Në prani të kontaminimit më të vogël, argjendi lirohet në formën e një sedimenti të lirshëm gri.
Reaksioni "pasqyrë argjendi" mund të përdoret si një reaksion cilësor për aldehidet. Kështu, reagimi i "pasqyrës së argjendtë" mund të përdoret si një dallues midis tyre glukozë Dhe fruktoza. Glukoza është një aldozë (përmban një grup aldehid në një formë të hapur), dhe fruktoza është një ketozë (përmban një grup keto në një formë të hapur). Prandaj, glukoza jep një reagim "pasqyrë argjendi", por fruktoza jo. Por nëse një medium alkalik është i pranishëm në tretësirë, atëherë ketozat izomerizohen në aldoza dhe gjithashtu japin reaksione pozitive me një tretësirë amoniaku oksid argjendi (Reagent Tollens).
Reagimi cilësor i glukozës me një zgjidhje amoniaku të oksidit të argjendit. Prania e një grupi aldehidi në glukozë mund të vërtetohet duke përdorur një zgjidhje amoniaku të oksidit të argjendit. Shtoni tretësirën e glukozës në tretësirën e amoniakut të oksidit të argjendit dhe ngrohni përzierjen në një banjë uji. Së shpejti argjendi metalik fillon të depozitohet në muret e balonës. Ky reagim quhet reagimi i pasqyrës së argjendit. Përdoret si një përbërje cilësore për zbulimin e aldehideve. Grupi aldehid i glukozës oksidohet në një grup karboksil. Glukoza shndërrohet në acid glukonik.
CH 2 AI - (SNON) 4 – GJUM +Ag 2 O= CH 2 AI - (SNON) 4 – COOH + 2Ag↓

Rendi i punës.
2 ml hidhet në dy epruveta. tretësirë amoniaku e oksidit të argjendit. Njërës prej tyre i shtoni 2 ml. 1% zgjidhje glukoze, tjetra - fruktozë. Të dy epruvetat po vlojnë.
Një zgjidhje amoniaku e hidratit të oksidit të argjendit përftohet duke reaguar nitratin e argjendit me hidroksid natriumi dhe hidroksid amoniumi:
AgNO3+ NaOH → AgOH↓+ NaNO3,
AgOH + 2 NH4 OH→[ Ag(NH3)2] OH + H2O,
zgjidhje amoniaku
OH + 3 H2→ Ag2O + 4 NH4 OH.
Parimi i metodës. Në muret e epruvetës formohet një pasqyrë me glukozë si rezultat i çlirimit të argjendit metalik.
Hartimi i punës: Shkruani në një fletore përfundimin, si dhe rrjedhën dhe ekuacionet e reaksionit.
Eksperimenti 3. Reagimi cilësor ndaj fruktozës
Parimi i metodës. Kur ngrohni një mostër që përmban fruktozë në prani resorcinol Dhe të acidit klorhidrik deri në 80 o C pas disa kohësh shfaqet një ngjyrë e kuqe e ndezur në epruvetën me fruktozë.
Kur ngrohni një mostër që përmban fruktozë në prani resorcinol Dhe të acidit klorhidrik shfaqet një ngjyrë e kuqe vishnje. Mostra është gjithashtu e aplikueshme për të zbuluar të tjera ketoza. Aldose në të njëjtat kushte, ato ndërveprojnë më ngadalë dhe japin një ngjyrë rozë të zbehtë ose nuk ndërveprojnë fare. Hapur F. F. Selivanov në 1887. Përdoret për analizën e urinës. Testi është pozitiv për fruktouri me origjinë metabolike ose transportuese. Në 13% të rasteve, testi rezulton pozitiv me një ngarkesë ushqimore me fruta dhe mjaltë. Kimik. formulë fruktoza – C 6 H 12 O 6
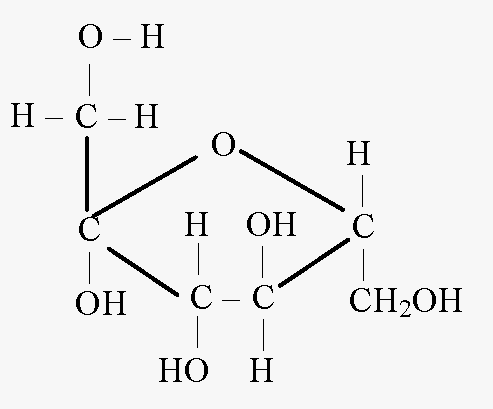
Formula ciklike e fruktozës
Forma aciklike 
fruktoza
Lidhje e lyer
R- mbetjet
hidroksimetilfurfural
Rendi i punës.
2 ml derdhen në dy epruveta: në njërën - një zgjidhje glukoze 1%, në tjetrën - një zgjidhje fruktoze 1%. Në të dy epruvetat shtohen 2 ml reagent Selivanov: 0,05 g resorcinol tretet në 100 ml acid klorhidrik 20%. Të dy epruvetat ngrohen me kujdes në 80 o C (para zierjes). Shfaqet një ngjyrë e kuqe.

Përfundime: rezultatet e eksperimentit dhe ekuacioni i reagimit shkruhen në një fletore.
Le të vazhdojmë temën e eksperimenteve kimike, sepse shpresojmë se do t'ju pëlqejnë patjetër. Këtë herë ju paraqesim një tjetër eksperiencë magjepsëse, gjatë së cilës do të marrim një pasqyrë argjendi.
Le të fillojmë duke parë videon
Do të na duhen:
- kapaciteti;
- nitrat argjendi;
- ujë i nxehtë;
- tretësirë amoniaku 10%;
- glukozë;
- djegës me alkool

Le të fillojmë me nitratin e argjendit. Merrni rreth një gram prej tij dhe holloni në një sasi të vogël uji të nxehtë.

Më pas, shtoni hidroksid natriumi në tretësirën që rezulton. Gjatë këtij reaksioni formohet oksidi i argjendit, i cili precipiton.

Më pas, shtoni një zgjidhje 10 për qind të amoniakut në precipitatin e oksidit të argjendit. Tretësira e amoniakut duhet të shtohet derisa precipitati të tretet.

Gjatë këtij reagimi, formohet amoniak argjendi. Shtoni 5 gram glukozë në tretësirën që rezulton.

Tani ju duhet të ngrohni përzierjen që rezulton. Për ta bërë këtë, ndizni djegësin e alkoolit dhe vendosni gotën mbi të në mënyrë që përzierja të nxehet gradualisht. Gjatë këtij reagimi, një sasi shumë e madhe e amoniakut lirohet, kështu që ky reagim duhet të kryhet ose nën kapuç ose jashtë. Gjatë reaksionit mund të formohet edhe nitriti i argjendit, i cili është një substancë shumë e rrezikshme, ndaj enët duhet të lahen mirë pas reaksionit.


Pas ca kohësh, një shtresë e hollë argjendi gradualisht fillon të vendoset në muret e xhamit. Reagimi përfundon afërsisht 15 minuta pas fillimit të ngrohjes.


Për të marrë një shtresë më të barabartë argjendi, duhet të vendosni një gotë me përzierjen në një enë të madhe, të derdhni ujë të nxehtë në enë dhe ta vendosni në një djegës alkooli. Temperatura kështu do të shpërndahet në mënyrë të barabartë dhe rezultati do të jetë më efektiv.


 Burri im nuk dëshiron të sigurojë familjen e tij
Burri im nuk dëshiron të sigurojë familjen e tij Zgjedhja e një modeli në modë të thonjve për Vitin e Ri Dreri i lezetshëm me sarafanë dhe shalle të kuqe - një manikyr i shkëlqyeshëm për një festë të Vitit të Ri rinor
Zgjedhja e një modeli në modë të thonjve për Vitin e Ri Dreri i lezetshëm me sarafanë dhe shalle të kuqe - një manikyr i shkëlqyeshëm për një festë të Vitit të Ri rinor Ne bëjmë topa dekorativë nga fijet dhe ngjitësi
Ne bëjmë topa dekorativë nga fijet dhe ngjitësi