銀鏡の反応をもとにどの演出が行われるのか。 化学実験:銀鏡の入手
作業の完了:
ホルマリン1mlを試験管に注ぎ、酸化銀のアンモニア溶液を少量加えた。 試験管を加熱した。 試験管の壁と底に銀が析出することを観察します。 ガラスの表面が反射するのは、鏡を作る原理によるものです。
実験 2. 大気中の酸素によるベンズアルデヒドの酸化
作業の完了:
ベンズアルデヒドを 1 滴、スライドガラス上に置き、空気中に 30 分間放置しました。 液滴の縁に沿って白い結晶が形成されるのが観察されます。 酸化反応が起こり、安息香酸が生成されました。

実験 3. 酢酸ナトリウムからのアセトンの調製
少量の酢酸ナトリウム粉末を試験管に入れ、ガス排出管を備えた栓で閉じた。 試験管をスタンドに取り付けた。 ガス出口管の端を水の入った試験管内に下げた。 酢酸ナトリウムの入った試験管を加熱した。 水の入った試験管内で気泡が放出されるのを観察すると、アセトンの特有の匂いが感じられます。 反応が停止したら、最初の試験管に濃塩酸を 1 滴加えます。 二酸化炭素の泡の放出が観察されます。
ガラスにミラーコーティングを形成する美しい効果の実験は非常に視覚的です。 この反応には経験と忍耐が必要です。 この記事では、必要かつ具体的な装置の準備について学び、このプロセスでどのような反応方程式が起こるのかも確認します。
銀鏡反応の本質は、アルデヒドの存在下で酸化銀のアンモニア溶液が相互作用する際の酸化還元反応の結果として金属銀が形成されることです。
「シルバーミラー」(左側の試験管)耐久性のある銀の層を作成するには、次のものが必要です。
- 最大100mlの容量を持つガラスフラスコ。
- アンモニア溶液 (2.5-4%);
- 硝酸銀(2%);
- ホルムアルデヒド水溶液(40%)。
代わりに、既製のTollens試薬(酸化銀のアンモニア溶液)を使用できます。 それを作成するには、1グラムの硝酸銀を10滴の水に加える必要があります(液体を長期間保存する場合は、暗い場所または暗い壁のガラス容器に置く必要があります)。 実験の直前に、溶液(約 3 ml)を 10% 水酸化ナトリウム水溶液と 1:1 の比率で混合する必要があります。 銀が沈殿する可能性があるため、アンモニア溶液をゆっくり加えて希釈します。 アンモニア溶液を使って別の素晴らしい実験を行い、「化学写真」を印刷することをお勧めします。
反応は室温で行われる。 最終的に成功するための前提条件は、ガラス容器の壁が完全にきれいで滑らかであることです。 壁に汚染物質のごくわずかな粒子がある場合、実験の結果得られた堆積物は黒または濃い灰色の緩い層になります。
フラスコを洗浄するには、さまざまな種類のアルカリ溶液を使用する必要があるため、処理のために溶液を採取し、洗浄後に蒸留水で洗い流す必要があります。 洗浄剤の入ったフラスコを何度も洗い流す必要があります。
容器の清潔さがなぜそれほど重要なのでしょうか?
実際のところ、実験の最後に形成された銀コロイド粒子はガラスの表面にしっかりと付着する必要があります。 表面に脂肪や機械粒子があってはなりません。 この水には塩が含まれていないため、フラスコの最終洗浄に最適です。 自宅で準備することもできますが、既製の液体を購入する方が簡単です。
銀鏡の反応式:
Ag₂O + 4 NH₃・Н₂О ⇄ 2ОН + 3Н₂О、
ここで、OH はジアンミン水酸化銀であり、金属酸化物をアンモニア水溶液に溶解することによって得られます。
 ジアミン銀錯体分子
ジアミン銀錯体分子
重要!反応は低濃度のアンモニアでも起こります - 比率を注意深く観察してください。
反応の最終段階は次のように進行します。
R (任意のアルデヒド)-CH=O + 2OH → 2Ag (沈降銀コロイド) ↓ + R-COONH4 + 3NH3 + H2O
反応の第 2 段階は、フラスコをバーナーの炎で慎重に加熱して行う方が良いです。これにより、実験が成功する可能性が高まります。
銀の鏡の反応は何を示しますか?
この興味深い化学反応は、物質の特定の状態を示すだけでなく、アルデヒドの定性測定にも使用できます。 つまり、このような反応は、溶液中にアルデヒド基が存在するかどうかという問題を解決することになります。
 アルデヒドの一般構造式
アルデヒドの一般構造式
たとえば、同様のプロセスで、溶液にグルコースが含まれているかフルクトースが含まれているかを調べることができます。 グルコースは肯定的な結果をもたらします - 「銀の鏡」が得られますが、フルクトースにはケトン基が含まれているため、銀の沈殿物を得ることができません。 分析を実行するには、ホルムアルデヒド溶液の代わりに 10% グルコース溶液を添加する必要があります。 溶解した銀が固体の沈殿物に変わる理由と仕組みを見てみましょう。
2OH + 3H₂O + C₆H₁₂O₆ (グルコース) = 2Ag↓+ 4NH₃・H₂O + C₆H₁₂O₇ (グルコン酸が生成される)。
銀鏡反応が何であるかを理解する必要がありますか? 銀鏡反応は、酸化銀のアンモニア溶液から金属銀を還元するプロセスです。
Ag2O + 4NH4OH ↔ 2OH + H2O
酸化銀はアンモニア水溶液に溶解して、錯体銀化合物、水酸化銀ジアミン (I) OH を形成します。
銀錯体化合物にアルデヒド(ホルムアルデヒド)を添加すると、酸化還元反応により金属銀が生成します。 反応の結果、ガラス試験管の壁に銀または鏡の美しい鏡面コーティングが形成されます。
R-CH=O + 2OH → 2Ag ↓ + R-COONH4 + 3NH3 + H2O
化学の教科書には、銀鏡反応をアルデヒドの検出に使用できると書かれています。 たとえば、グルコースは「銀の鏡」反応を示しますが、フルクトースは反応しません。 ただし、アルデヒドのように、銀鏡と反応する可能性のある化学物質が数多くあります。
実際に銀鏡反応を実行するにはどうすればよいでしょうか?
一見すると、銀鏡反応を行うのは非常に簡単であるように見えますが、これは完全に真実ではありません。 すべてが単純に思えました。アンモニア溶液にアルデヒドを加えたり、ホルムアルデヒドやグルコースの溶液を使用して、銀鏡反応を実行することができます。 しかし、これは銀鏡反応が何であるかを理解するための単純かつ原始的なアプローチです。 この反応は失望につながる可能性があります。 予想されるガラス上のミラーコーティングの代わりに、溶液中の銀の黒または茶色の懸濁液が形成される場合があります。通常、このような単純な方法での反応は失敗に終わることがほとんどです。 たとえ鏡を作成できたとしても、その品質は非常に低いものになります。 銀の層はもろくて不均一であることがわかります。 なぜこうなった? このような反応がうまくいかない理由はたくさんあります。 これらのうち、主な理由は 2 つあります。反応に必要な条件を満たしていないこと、または銀めっき用のガラス表面の準備が不十分であることです。
反応の結果、正に帯電した銀イオンが形成され、アルデヒド基と結合して小さな銀粒子またはコロイド状の銀粒子が形成されます。 このような小さな粒子はガラスの表面にしっかりと付着したり、銀の懸濁液の形で溶液中に残ることがあります。
コロイド銀粒子がガラスに確実に付着し、強力で均一な銀の層、つまり鏡を形成するには、銀メッキの前にまずガラス表面を脱脂する必要があります。 ガラスの表面は完全にきれいであるだけでなく、できるだけ滑らかである必要があります。
ガラスの主な汚染物質はグリースであり、これを除去する必要があります。 脂肪を除去するには、アルカリ溶液とホットクロム混合物を使用し、その後ガラスを蒸留水で繰り返し洗浄します。 アルカリがない場合は、最終手段として通常の食器用合成洗剤を使用できます。 脱脂後、ガラスを塩化第一スズと蒸留水の溶液ですすぐと効果的です。
すべての溶液は蒸留水で作成する必要があります。 蒸留水が入手できない場合、最後の手段として雨水を使用できます。 銀鏡反応で金属銀を還元するには、ホルムアルデヒドまたはグルコースなどの還元剤がよく使用されます。 これら 2 つの物質の選択は、化学反応が使用される目的によって異なります。
ホルムアルデヒドを用いた銀鏡反応
実験を実証するために、ホルムアルデヒドを関与させて銀鏡の反応を実行することができます。 耐久性があり均一な表面を備えた高品質の鏡を作成する必要がある場合は、ブドウ糖を使用することをお勧めします。銀ガラスには、銀塩である硝酸銀を含む銀を摂取することをお勧めします。 アンモニアとアルカリの溶液を硝酸銀に加えます。 ガラスへの銀の堆積はアルカリ溶液中で行われなければなりません。 この場合、アルカリ溶液が多すぎることも望ましくないため、多すぎてはなりません。 技術に応じて、銀鏡反応は室温または加熱時に行われます。
溶液が茶色に変わった場合、それは溶液中に銀の小さなコロイド粒子が形成されたことを意味します。 その後、還元された銀の薄い鏡面コーティングがガラスの表面に形成されます。 銀鏡の反応を行うのは非常に簡単ですが、高品質の鏡を入手するのは非常に困難です。 高品質の銀コーティング、つまり銀の鏡を得るには、多くの作業を費やす必要があり、慎重かつ非常に粘り強く行う必要があります。
実験のために、予備的な慣れと銀の鏡の反応が何であるかを調べる目的で、単に銀のガラスのガラスを使用することはできますか? この反応を実証する場合、結果はあまり品質の良くない鏡になる可能性があります。
反応を実行するには、容量 50 ~ 100 ml の清潔なガラス フラスコ、濃度 2.5 ~ 4 パーセントのアンモニア溶液、硝酸銀の 2 パーセント溶液、およびホルムアルデヒド溶液が必要です。
銀メッキの前に、化学反応のためにフラスコを準備します。 フラスコをブラシと石鹸で拭いて機械的不純物を取り除き、蒸留水ですすいでください。 次に、クロム混合物ですすぎ、さらに蒸留水ですすぎます。
2 パーセント溶液をフラスコの 4 分の 1 に注ぎ、この溶液にアンモニア溶液を徐々に加えます。 アンモニア溶液は、25%アンモニア溶液を蒸留水で8~10倍に希釈して調製します。 落下する沈殿が過剰に完全に溶解するまで、アンモニア溶液を硝酸銀に徐々に加えます。 形成された溶液に、壁に沿ってホルマリン溶液 - 0.5〜1 mlを徐々に加えます。 ガラスフラスコを熱湯、またはさらに沸騰したお湯の入った容器に置きます。 すぐにフラスコ上でそれが形成され始め、美しい銀色の鏡が形成されます。
この技術の主な欠点は、硝酸銀溶液にアンモニア溶液だけでなくアルカリ(水酸化ナトリウム - NaOH または水酸化カリウム - KOH)も添加する必要があることです。 高品質のミラーコーティングを得るには、まずアンモニアを添加し、次にアルカリを添加する必要があります。
銀鏡の反応を簡単に示すには、その逆を行うことができます。まず、茶色の沈殿物 (Ag2O) の形成が止まるまで硝酸銀にアルカリを加え、次に沈殿物が完全に溶解するまでアンモニア溶液を加えます。
2Ag+ + 2OH - = Ag2O + H2O
Ag2O + 4NH3 + H2O = 2OH
この手法を実行すると、白色の沈殿物が形成されることがありますが、おそらくそれはメテナミン (またはヘキサメチレンテトラミン) です。
6CH2O + 4NH3 = (CH2)6N4 + 6H2O
白い沈殿物の形成は悪い兆候であり、高品質の鏡を得るのには役立ちません。
銀鏡の反応は酸性環境ではなく、必然的にアルカリ性環境で起こる必要があることに特に注意する必要があります。 酸性環境では、銀コーティングが形成されずに銀ミラーの反応が起こります。 試薬を混合すると、媒体が突然酸性になる場合があります。 反応混合物に過剰なアルカリを加えるだけで、すぐにガラス試験管の壁に銀色の鏡が形成されます。
グルコースを用いた銀鏡反応
グルコースを使用した銀鏡反応は、化学反応を実証するためだけでなく、高品質の銀鏡や導電性表面を得るためにも実行できます。銀鏡反応は、酸化銀のアンモニア溶液 (トーレンス試薬) から金属銀を還元する化学プロセスであることは誰もがよく知っています。
銀鏡反応は銀鏡の製造の基礎です。 金属銀(Ag)が酸化して黒くなる(Ag2S)、つまりくすんだり傷がついたりするのを防ぐために、保護ニスでコーティングされています。 鏡を銀色にするには、新たに調製した 2 つの溶液 (A と B) を準備する必要があります。
解決策 - A
100 ml の蒸留水に 6 グラムの硝酸銀 (AgNO3) を溶解し、最初に形成された沈殿が溶解するまでこの溶液にアンモニア水溶液を加えます。 次に、得られた溶液にアルカリ、つまり水酸化ナトリウム(NaOH)の3パーセント溶液70mlを加え、溶液が完全に透明になるまで(過剰になることなく)アンモニア水溶液を再び注ぎます。 得られた溶液を蒸留水で500mlに希釈する。解決策 – B
25 ml の蒸留水に 1.3 グラムのグルコースを溶解し (得られた溶液に濃硝酸 - HNO3 を 1 滴加えます)、得られた溶液を 2 分間沸騰させます。 次に、溶液を冷却し、同量のアルコールで希釈します。解決策: 使用直前に A と B を 10:1 の比率で混合します。 溶液を混合すると、30 分以内にガラス上に銀の厚い膜が形成されます。
鏡を銀色にする前に、ガラスをよく掃除する必要があります。 これは非常に重要かつ必要な条件です。 高品質なミラーコーティングを得るには、この条件を無視することはできません。 ガラス表面は、HNO3 + K2Cr2O7 の高温混合物で洗浄され、その後、ガラスは蒸留水ですすぎ、アルコールで処理されます。
より厚い銀の層を得るために、新たに調製した溶液を用いて銀ガラスの表面処理をさらに 1 ~ 2 回繰り返します。 次に、水とアルコールで洗浄すると、銀の沈殿が形成されます。
スクロースを用いた銀鏡反応
銀鏡反応は、スクロースの関与により(ホルムアルデヒドまたはグルコースが存在しない場合)実行できます。 反応前に、濃度 10% に希釈した硫酸と硝酸を使用してスクロースを加水分解します。 酸溶液を砂糖水溶液に、砂糖 100 グラムあたり酸 10 ml の割合で加えます。 得られた溶液を15〜20分間沸騰させます。 加水分解を受けると、スクロースはグルコースとフルクトースの混合物になります。でんぷんを用いた銀鏡反応
反応にグルコースの代わりにデンプンを使用すると失敗につながります。 これは、加水分解の結果、デンプンが完全にはグルコースに変換されないために起こります。 このデンプンの部分加水分解により、デキストリン、つまりデンプンと同様にデンプンとは異なり、より分子量の低いグルコース単位からなる多糖類が形成されます。 デキストリンは鎖の末端に銀イオンを還元するアルデヒド基を持っていますが、これにより期待されるミラーコーティングではなく、黒色の銀コロイド溶液が生成されます。 金属銀はガラス表面に沈降しません。これは、デキストリンの長い線状分子が銀コロイド溶液を安定化させるためと思われます。 言い換えれば、これらの分子は保護コロイドの機能を果たします。 銀の黒色コロイド溶液の形成を防ぐためには、デンプンを完全に加水分解する必要があります。実験室ワークNo.5
プロパティ炭水化物
実験1. 銀鏡の反応回復反応です 銀アンモニア溶液から 酸化銀 (トーレンズ試薬).
水溶液中 アンモニア酸化銀は溶解して複雑な化合物を形成します - 水酸化ジアンミン銀(I) OH
どちらに追加すると アルデヒド酸化還元反応が発生して金属銀が形成されます。
反応が清潔で滑らかな壁を備えた容器内で行われると、銀が薄膜の形で沈殿し、鏡面が形成されます。
わずかな汚染があると、銀が灰色の緩い沈殿物の形で放出されます。
「銀鏡」反応は、アルデヒドの定性反応として使用できます。 したがって、「銀の鏡」反応は、 グルコースそして フルクトース。 グルコースはアルドース(開いた形でアルデヒド基を含む)であり、フルクトースはケトース(開いた形でケト基を含む)です。 したがって、グルコースは「銀の鏡」反応を示しますが、フルクトースは反応しません。 しかし、溶液中にアルカリ性媒体が存在すると、ケトースはアルドースに異性化され、アンモニア溶液との陽性反応も生じます。 酸化銀 (トーレンズ試薬).
グルコースと酸化銀のアンモニア溶液との定性的反応。グルコース中のアルデヒド基の存在は、酸化銀のアンモニア溶液を使用して証明できます。 酸化銀のアンモニア溶液にグルコース溶液を加え、混合物を水浴中で加熱します。 すぐに金属銀がフラスコの壁に堆積し始めます。 この反応は銀鏡反応と呼ばれます。 アルデヒドの発見のための高品質の化合物として使用されます。 グルコースのアルデヒド基が酸化されてカルボキシル基になります。 グルコースはグルコン酸に変換されます。
CH 2 彼 – (スノン) 4 – 睡眠 +銀 2 ○=CH 2 彼 – (スノン) 4 – COOH + 2銀↓

仕事の順番。
2mlを2つの試験管に注ぎます。 酸化銀のアンモニア溶液。 そのうちの1つに2mlを加えます。 1%ブドウ糖溶液、もう1つはフルクトースです。 両方の試験管が沸騰しています。
酸化銀水和物のアンモニア溶液は、硝酸銀を水酸化ナトリウムおよび水酸化アンモニウムと反応させることによって得られます。
AgNO3+NaOH→AgOH↓+NaNO3、
AgOH + 2 NH4 OH→[Ag(NH3)2] OH + H2O、
アンモニア溶液
OH + 3 H2→ Ag2O + 4 NH4 OH。
メソッドの原理。 金属銀の放出の結果として、グルコースを含む試験管の壁に鏡が形成されます。
作業の設計: 結論、反応の経過と方程式をノートに書きます。
実験3. フルクトースに対する定性反応
メソッドの原理。 果糖を含む試料を存在下で加熱する場合 レゾルシノールそして 塩酸の 80℃までは、フルクトースを含む試験管内でしばらくすると明るい赤色が現れます。
果糖を含む試料を存在下で加熱する場合 レゾルシノールそして 塩酸のチェリーレッドの色が現れます。 このサンプルは他の検出にも適用できます。 ケトーシス. アルドース同じ条件下では、よりゆっくりと相互作用して淡いピンク色になるか、まったく相互作用しません。 開ける F.F.セリバノフ 1887年に。 尿の分析に使用されます。 この検査は、代謝または輸送起源のフルクト尿症について陽性です。 果物や蜂蜜を大量に摂取すると、13% のケースで検査が陽性となります。 化学。 式フルクトース – C 6 H 12 O 6
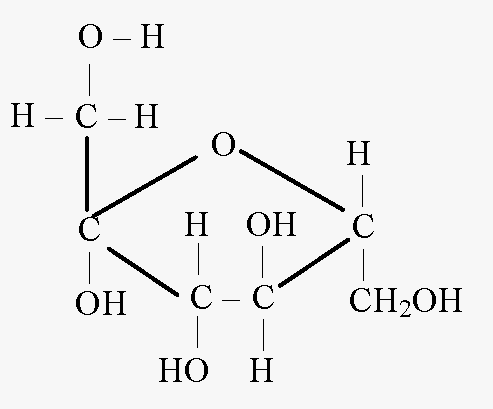
フルクトースの環状式
非環状形式 
フルクトース
塗装された接続部
R-残基
ヒドロキシメチルフルフラール
仕事の順番。
2mlを2つの試験管に注ぎます:一方には1%グルコース溶液、もう一方には1%フルクトース溶液。 セリバノフ試薬 2 ml を両方の試験管に加えます。レゾルシノール 0.05 g を 20% 塩酸 100 ml に溶解します。 両方の試験管を慎重に 80℃ (沸騰前) に加熱します。 赤い色が現れます。

結論: 実験の結果と反応式をノートに書き留めます。
化学実験の話題を続けてみましょう。きっと皆さんに気に入っていただけると思います。 今回は、銀の鏡を受け取る別の魅力的な体験を皆さんにご紹介します。
まずはビデオを見てみましょう
必要なものは次のとおりです。
- 容量;
- 硝酸銀;
- お湯;
- 10%アンモニア溶液;
- ブドウ糖;
- アルコールバーナー

硝酸銀から始めましょう。 1グラム程度をとり、少量のお湯で薄めてください。

次に、得られた溶液に水酸化ナトリウムを加えます。 この反応中に酸化銀が形成され、沈殿します。

次に、10 パーセントのアンモニア溶液を酸化銀の沈殿物に加えます。 アンモニア溶液は、沈殿物が溶解するまで添加する必要があります。

この反応中に、アンモニア銀が形成されます。 得られた溶液に5グラムのグルコースを加えます。

次に、得られた混合物を加熱する必要があります。 これを行うには、アルコールバーナーに点火し、その上にガラスを置き、混合物が徐々に加熱されるようにします。 この反応中に非常に多量のアンモニアが放出されるため、この反応はフードの下または屋外で実行する必要があります。 反応中に亜硝酸銀も生成する可能性があり、これは非常に危険な物質であるため、反応後は皿をよく洗う必要があります。


しばらくすると、銀の薄い層が徐々にガラスの壁に沈み始めます。 加熱開始から約15分で反応は終了します。


より均一な銀の層を得るには、混合物を入れたガラスを大きな容器に入れ、容器に熱湯を注ぎ、アルコールバーナーの上に置きます。 これにより、温度が均一に分散され、より効果的な結果が得られます。


 磁器婚式おめでとうございます(結婚20周年)
磁器婚式おめでとうございます(結婚20周年) 友人への最高の詩の願い
友人への最高の詩の願い ソビャニンの「タイル熱」ロシア正教会の花崗岩
ソビャニンの「タイル熱」ロシア正教会の花崗岩 青少年の身長と体重の関係の特徴
青少年の身長と体重の関係の特徴